
Источник: Портал PaxForex Premium Analytics, Фундаментальная Информация
Обратный отсчет начался и речь идет не о выборах президента в США. Многие американцы с нетерпением ждут результатов первого раунда вакцины против коронавирусов, находящихся на поздней стадии тестирования.
Положительные клинические результаты должны привести к относительно быстрому получению разрешения на экстренное использование (EUA) от Управления по контролю за продуктами и лекарствами. Не исключено, что в течение ближайших нескольких месяцев безопасные и эффективные вакцины станут доступны на всей территории США. Это может стать поворотным моментом в борьбе с пандемией, которая до настоящего времени унесла более 200 000 жизней по всей стране и серьезно подорвала экономику.
Pfizer американская компания, которая, по всей вероятности, сначала объявит результаты тестирования своих соответствующих кандидатов на вакцину на поздней стадии. Но что, если результаты будут опубликованы с опозданием? Хотите верьте, хотите нет, но задержки на самом деле могут быть отличной новостью.
Компания Pfizer и ее партнер, немецкая биотехнология BioNTech, 27 июля 2020 года начали третью фазу клинического исследования кандидата на вакцину BNT162b2. Компании заявили в то время, что они могут обратиться за регуляторной проверкой уже в октябре, если испытания пройдут успешно.
12 сентября компании Pfizer и BioNTech предложили расширить поздний этап исследования BNT162b2, включив в него 44 000 участников вместо первоначально запланированных 30 000 участников. Однако это не повлияло на их ожидаемый график. Компания Pfizer и BioNTech подтвердили, что они " по-прежнему ожидают, что окончательные данные об эффективности, скорее всего, будут получены к концу октября".
Есть еще два производителя лекарств с кандидатами на вакцину, которые находятся на поздней стадии тестирования в США - AstraZeneca и Johnson & Johnson. Тем не менее, тестирование AstraZeneca в США все еще приостановлено из-за тяжелой реакции с участником клинических испытаний компании в Великобритании. Компания J&J начала 3-ю фазу тестирования своего кандидата на вакцину COVID-19 менее двух недель назад и ожидает результатов только в начале 2021 года.
Вы можете подумать, что любые задержки для Pfizer автоматически будут плохими новостями - но есть вероятность того, что потенциальные задержки могут стать отличной новостью.
Как? Все сводится к тому, что FDA потребует для предоставления EUA.
FDA планирует в ближайшее время выпустить руководство о критериях, которым должна удовлетворять вакцина для получения разрешения на экстренное использование. Хотя подробности пока неизвестны, были утечки информации о некоторых вероятных требованиях.
Особенно выделяются два из этих потенциальных критериев. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), вероятно, потребует, чтобы участники поздних клинических исследований кандидатов на вакцину находились под наблюдением в течение двух месяцев после получения второй дозы вакцины. Кроме того, ожидается, что агентство потребует, чтобы группы плацебо, участвующие в исследованиях, имели, по крайней мере, пять случаев тяжелой формы COVID-19.
Компания Pfizer может контролировать, как она соответствует первому из этих двух критериев, но если в группе плацебо не будет достаточно участников, у которых развиваются тяжелые случаи заболевания, то они не смогут обратиться в EUA.
Если такой сценарий произойдет, то это будет означать, что почти все невакцинированные лица, участвовавшие в поздних исследованиях, не будут заражены коронавирусом. Это было бы фантастично и свидетельствовало бы о значительном улучшении воздействия COVID-19 на страну. Это также означало бы, что у компании Pfizer будет больше вакцинированных участников для оценки профилей безопасности их соответствующих вакцин. Это могло бы повысить доверие американцев к вакцинам.
Конечно, существует также вероятность того, что компания Pfizer могут отложить объявление результатов на поздней стадии по внутренним причинам, таким как потребность в большем количестве времени для сбора и анализа данных. Этот сценарий не обязательно будет поводом снижения цены на акции, хотя он, скорее всего, повлияет на цены так или иначе.
Шансы на то, что Pfizer достигнет объявленных сроков представления результатов на поздней стадии для своих кандидатов на вакцину, почти наверняка высоки. Было бы почти чудом, если бы очень немногие участники групп плацебо компаний не смогли быть диагностированы тяжелые случаи COVID-19.
Следует помнить, что компания также знает, что на кону. Крупные внутренние ошибки, которые могут задержать объявление их результатов, должны быть маловероятны.
Компания Pfizer и BioNTech получат от правительства США 1,95 миллиарда долларов на поставку 100 миллионов доз BNT162b2, если вакцина получит EUA от FDA. Соглашение о поставках может быть расширено еще на 500 миллионов доз.
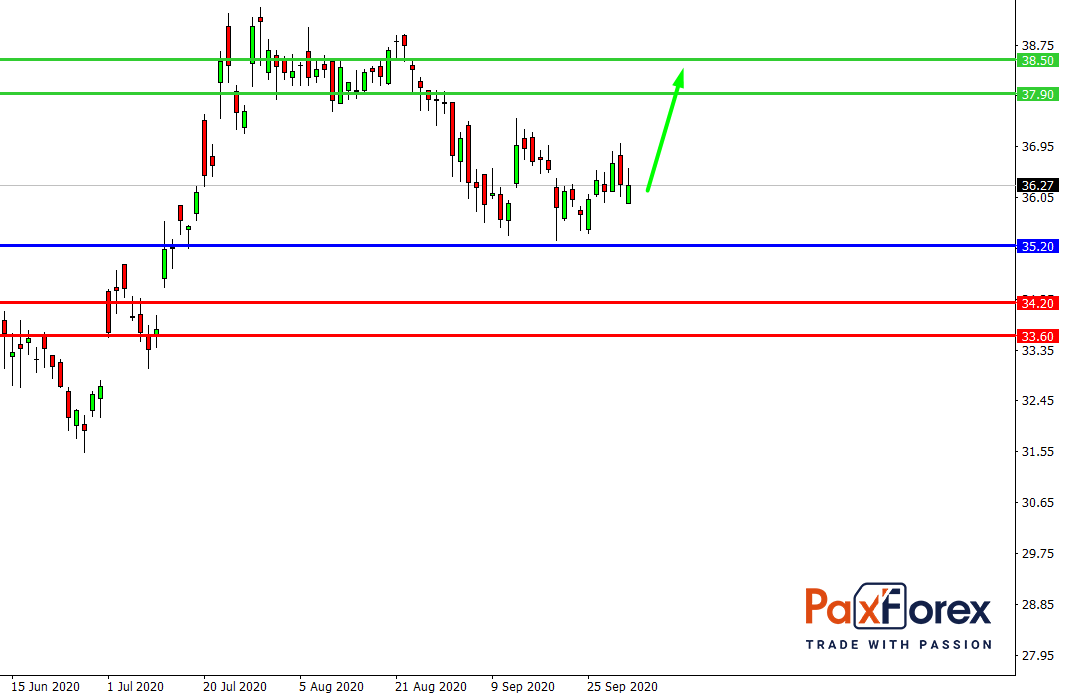
Пока цена находится выше уровня 35.20 следуйте рекомендациям ниже:
- Временной интервал: D1
- Рекомендация: длинная позиция
- Точка входа: 36.38
- Тейк-профит 1: 37.90
- Тейк-профит 2: 38.50
Альтернативный сценарий:
При пробое уровня 35.20 следуйте рекомендациям ниже:
- Временной интервал: D1
- Рекомендация: короткая позиция
- Точка входа: 35.20
- Тейк-профит 1: 34.20
- Тейк-профит 2: 33.60










